Souhaitez-vous quitter le site ?
Vous allez quitter le site www.cancer-supporters.fr et être redirigé vers un site externe. Amgen France n'est pas responsable du contenu présent sur ce site.
Les différents stades et grades
-
1
-
Les différents stades et grades - 2
-
3
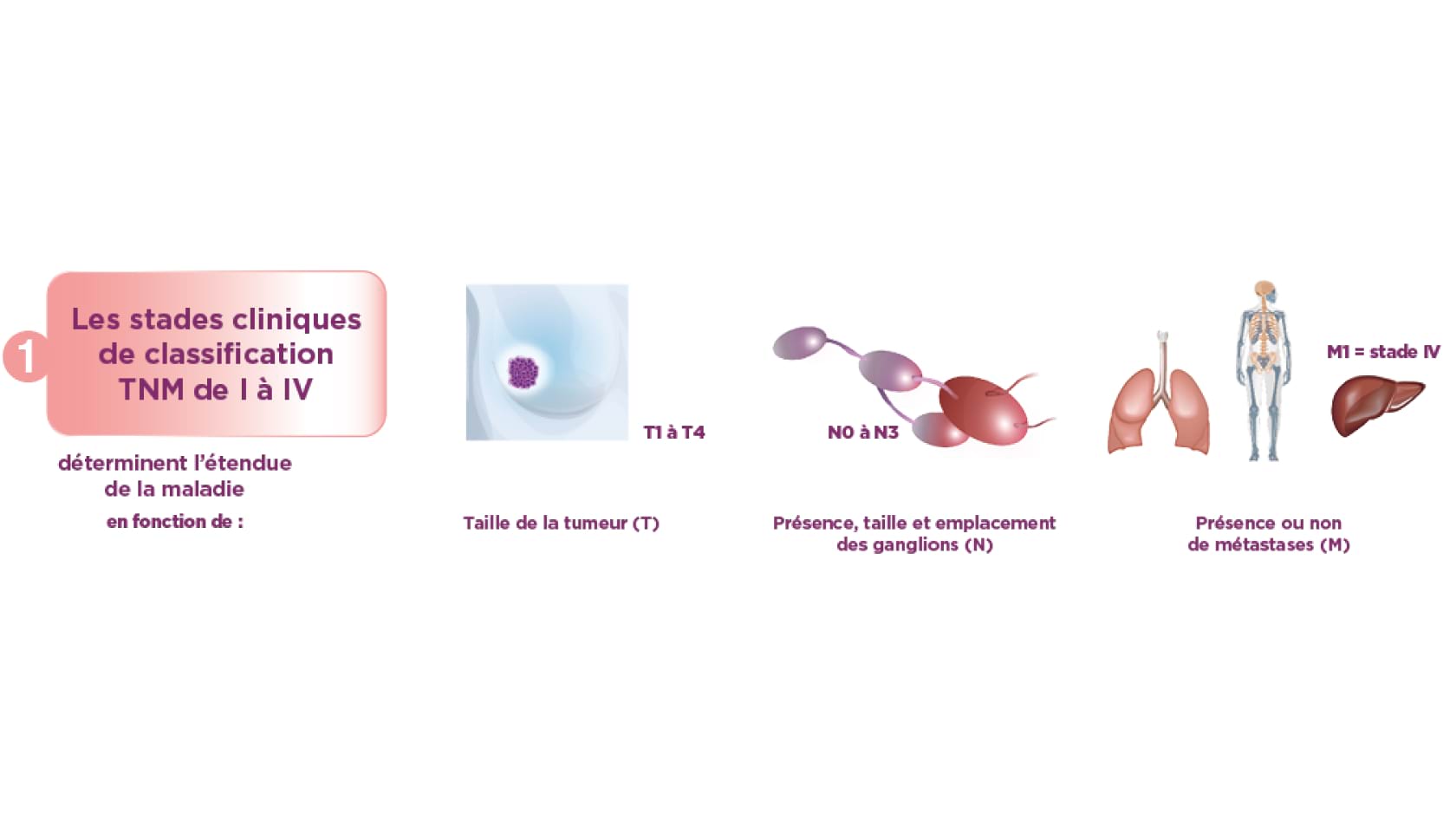

1 Les stades TNM : Il est possible de déterminer le stade, c’est-à-dire l’étendue du cancer. Pour cela, les médecins prennent en compte trois critères : la taille et l’infiltration de la tumeur (T) qui va de T0 (tumeur primitive non palpable) à T4 (tumeur étendue ou inflammatoire), l’atteinte des ganglions lymphatiques (N) qui va de N0 (pas de ganglions palpables) à N3 (ganglions fixés ou sus-claviculaires), et la présence (M1) ou non de métastases (M0)1.
Le stade des cancers du sein est exprimé par un chiffre romain allant de 0 à IV1.
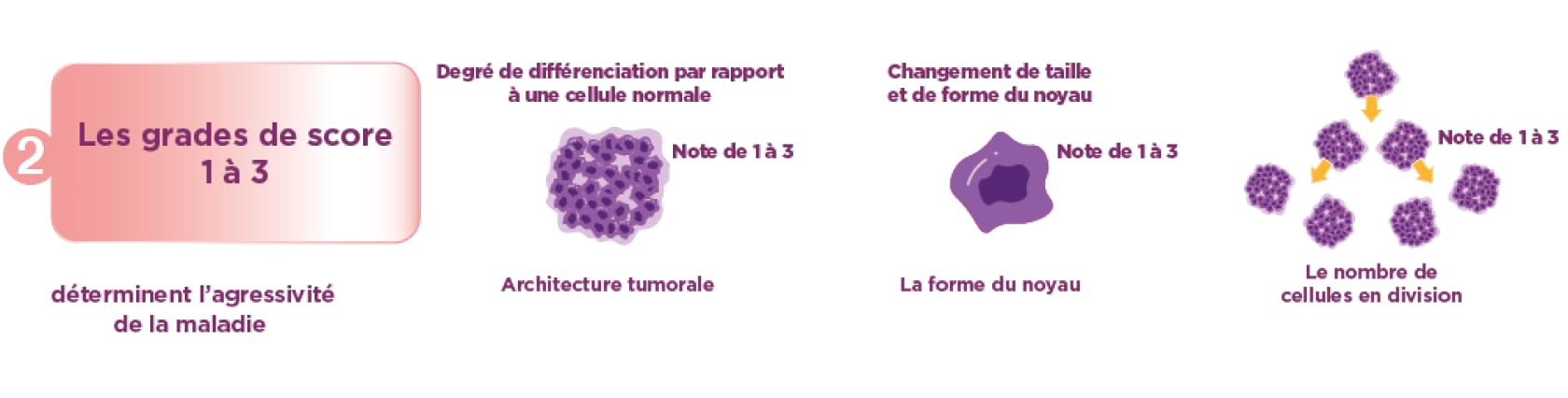
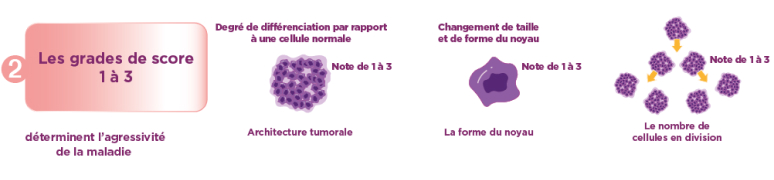
2 Les grades de
sévérité8 :
Le grade de sévérité de la tumeur exprime l’agressivité du cancer et est défini selon 3 critères : la structure
des cellules cancéreuses (proche ou non des cellules normales), le changement de la taille et la forme du noyau,
le nombre de cellules tumorales en division, c’est-à-dire la vitesse de multiplication des cellules.
À partir de cela, on peut distinguer 3 grades :
- Le grade I correspond aux tumeurs les moins agressives (structure bien formée, petits noyaux uniformes et division lente),
- Le grade II est un grade intermédiaire,
- Le grade III correspond aux tumeurs les plus agressives (peu ou pas de structure, gros noyaux non uniformes, division cellulaire rapide).


3 Le test génomique2 : Il s’agit de l’analyse d’un échantillon de la tumeur. Le niveau d’expression de plusieurs gènes est étudié pour déterminer si le risque de dissémination à distance est faible ou élevé. Ces tests peuvent être utilisés chez les patientes avec un cancer du sein précoce, RH+ et HER2-.
Les sous-types de cancers du sein
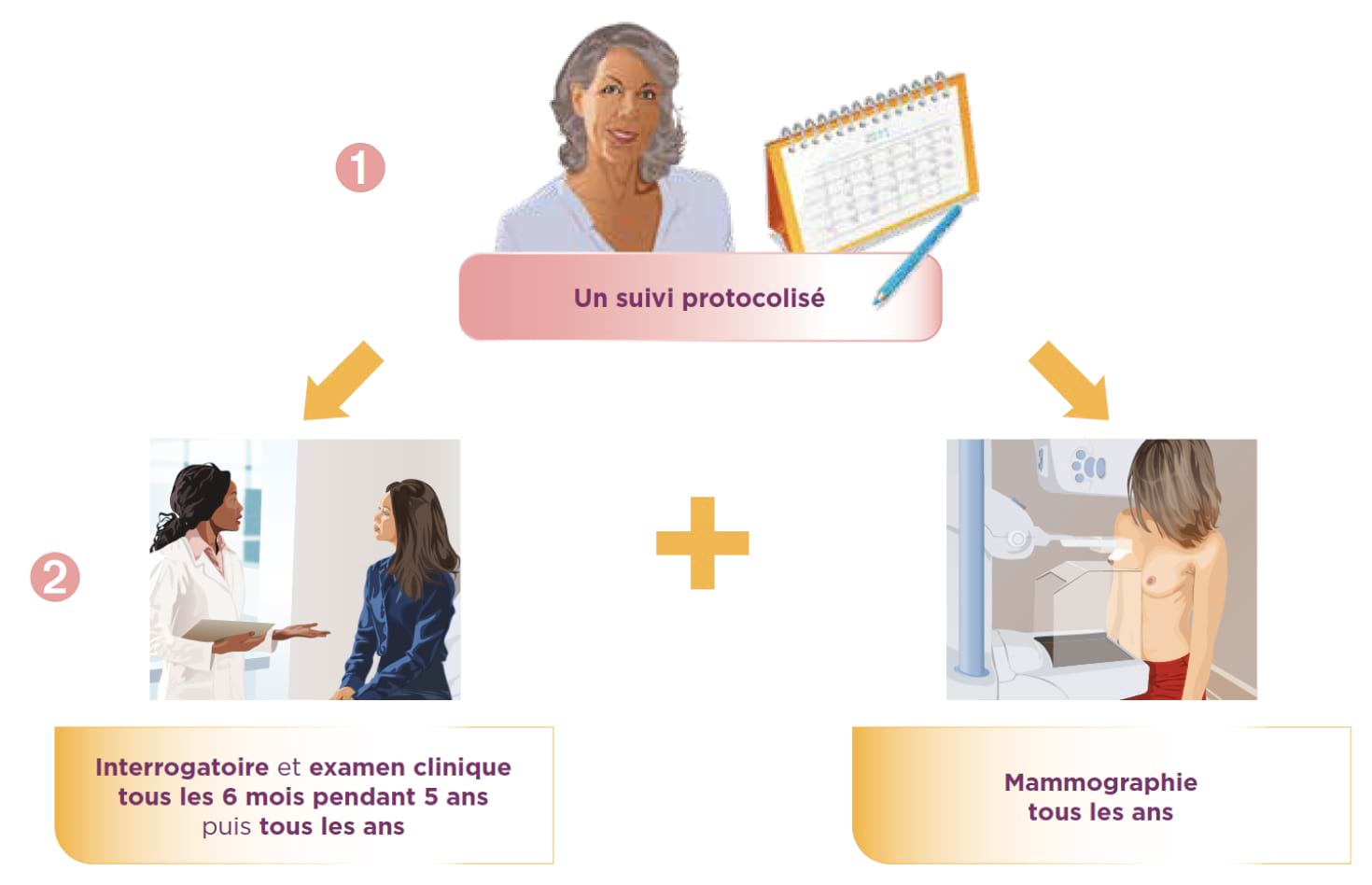
Le suivi
- Des consultations médicales régulières plusieurs fois par an pendant 5 ans, puis une fois par an. Les consultations médicales recherchent l’apparition de complications liées au traitement, des signes d’appel de récidive locale ou à distance et en évaluent l’évolution.
- Une mammographie bilatérale (ou unilatérale après mastectomie totale) est réalisée tous les ans et constitue l’examen de référence. D’autres examens peuvent être indiqués selon les traitements ou cas de présence de signes d’appel.
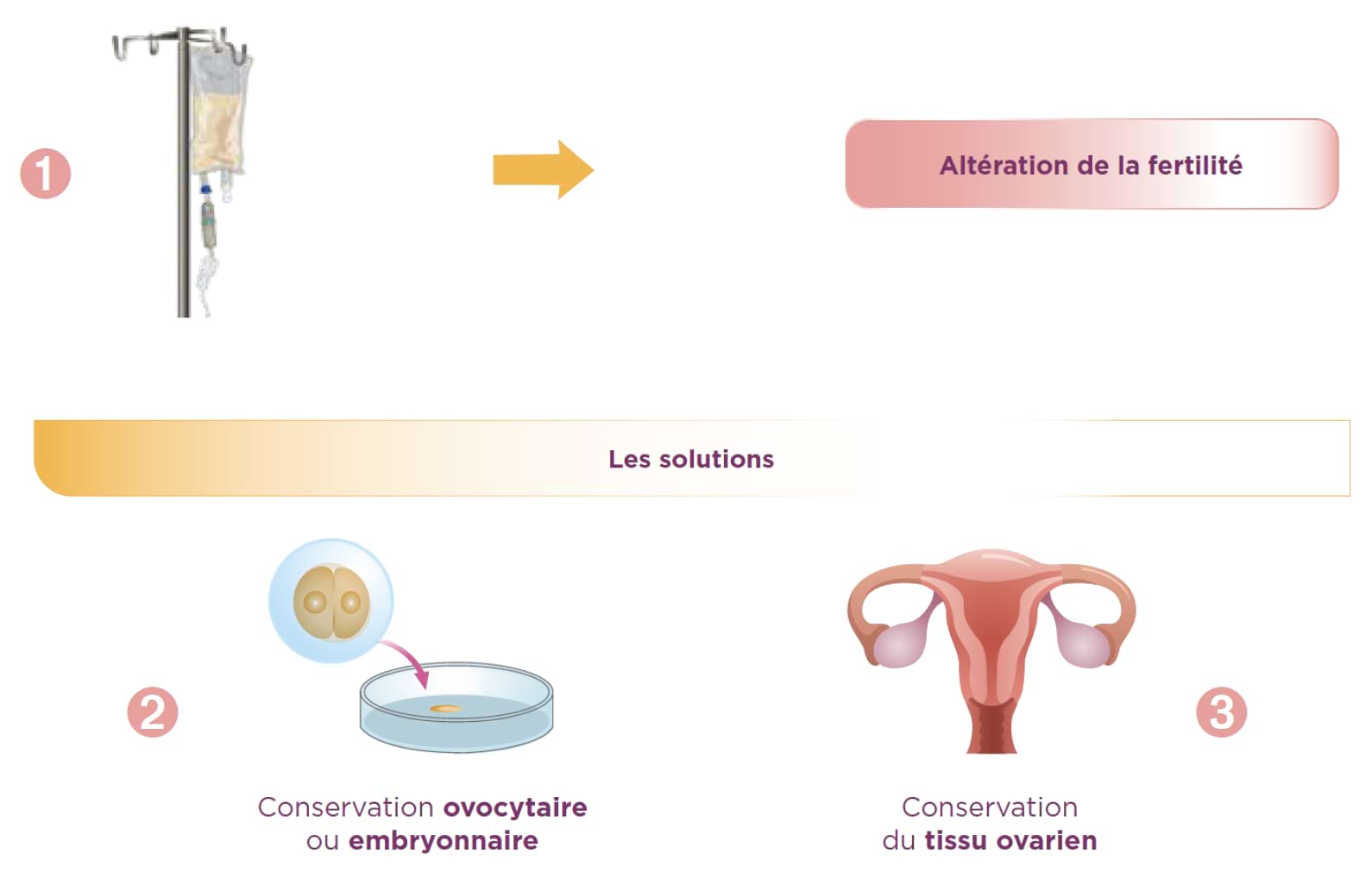
Préservation de la fertilité
Hérédité et cancer du sein
-
Hérédité et cancer du sein - 1
-
Hérédité et cancer du sein - 2
-
Hérédité et cancer du sein - 3
-
Hérédité et cancer du sein - 4
-
Hérédité et cancer du sein - 5


1 Il ne faut pas confondre susceptibilité familiale et prédisposition génétique.


2 Notre patrimoine génétique est constitué de 30 à 40 000 gènes. Parmi eux, deux gènes ont été identifiés comme étant particulièrement importants dans le développement des cancers du sein : BRCA1 et BRCA2 (BReast CAncer, cancer du sein en anglais). D’autres gènes peuvent être impliqués moins fréquemment comme TP53, PALB2, etc7.

3 Les analyses génétiques permettent de rechercher si une personne est porteuse d’un gène modifié pouvant favoriser le développement d’un cancer du sein ou de l’ovaire. Ces analyses sont proposées s’il existe une histoire personnelle et/ou familiale évoquant une prédisposition génétique7.


4 Dépistage plus précoce7
La surveillance et les examens de dépistage ne permettent pas d’empêcher l’apparition d’un cancer mais ont pour but de déceler et de prendre en charge un éventuel cancer le plus tôt possible.
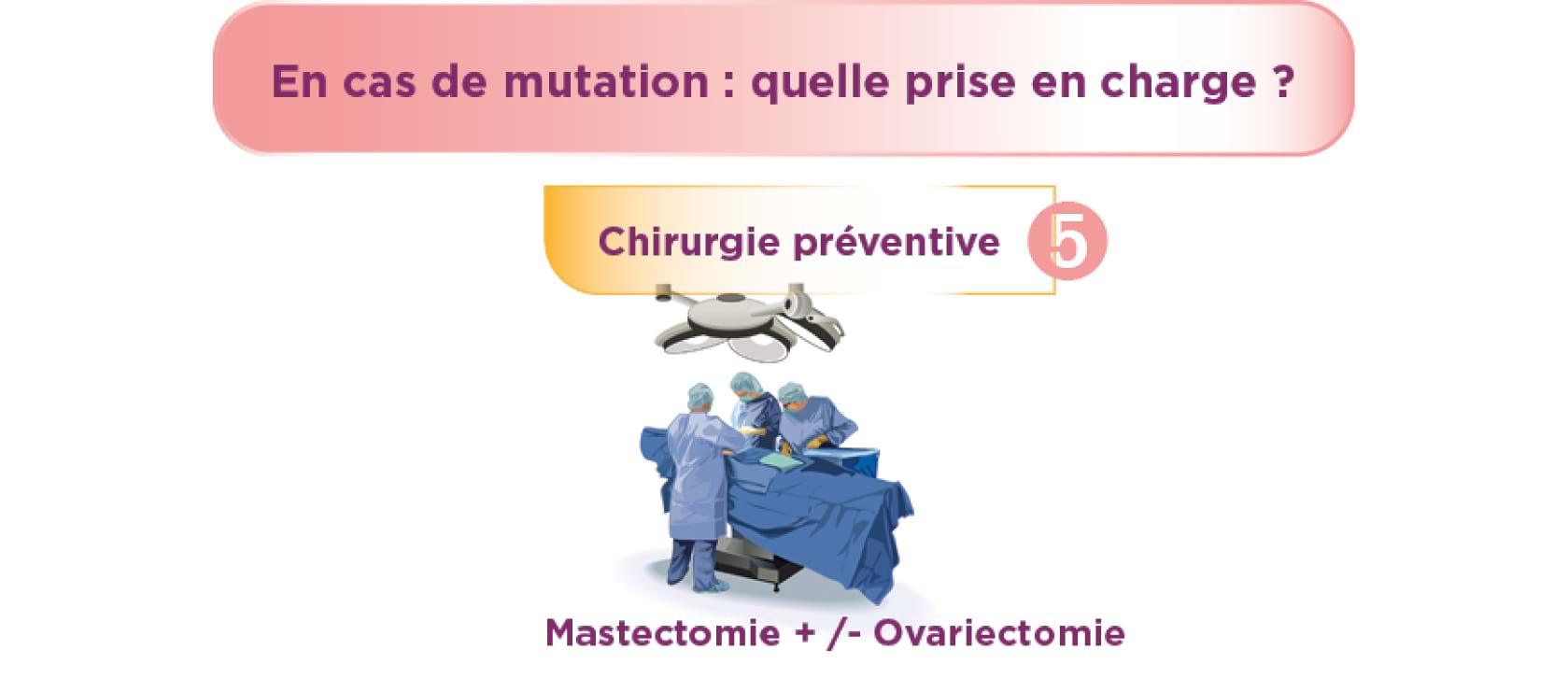
5 Chirurgie préventive7
Mastectomie : Pour être efficace, la mastectomie préventive doit enlever la totalité ou la quasi-totalité du tissu mammaire dans lequel un cancer risque de se développer. Bien qu’elle n’apporte pas une protection absolue contre le risque de cancer du sein, cette intervention préventive permet de diminuer le risque de survenue de 90%. Elle ne permet par ailleurs pas de prévenir l’apparition d’un cancer sur un autre organe, qu’il soit prédisposé par le même gène ou non.
-
Références
- INCa. Les stades du cancer. Mis à jour le 04/11/2020. Consulté le 18/03/2025. Disponible sur : https://www.cancer.fr/personnes-malades/les-cancers/sein/comprendre-les-cancers-du-sein/developpement-des-cancers-du-sein/les-stades-du-cancer
- Mon Réseau Cancer. Tests génomiques pour les cancers du sein : prédire le risque de récidive et préciser la nécessité ou non d'une chimiothérapie. Mis à jour le 30/10/2024. Consulté le 18/03/2025. Disponible sur : https://monreseaucancer.org/ressources/article/tests-genomiques-predire-le-risque-de-recidive-et-preciser-la-necessite-dun-ch
- Les traitements des cancers du sein, collection Guides patients Cancer info, INCa, Octobre 2013. INCa. Le suivi. Mis à jour le 04/11/2020. Consulté le 18/03/2025. Disponible sur : https://www.cancer.fr/personnes-malades/les-cancers/sein/la-qualite-de-vie/le-suivi
- INCa. Le suivi. Mis à jour le 04/11/2020. Consulté le 18/03/2025. Disponible sur : https://www.cancer.fr/personnes-malades/les-cancers/sein/la-qualite-de-vie/le-suivi
- Conséquences des traitements des cancers et préservation de la fertilité. Etat des connaissances et propositions. Agence de la Biomédecine et INCa. Février 2013.
- INCa. Prédispositions génétiques. Mis à jour le 04/11/2020. Consulté le 16/06/2025. Disponible sur : https://www.cancer.fr/personnes-malades/les-cancers/sein/comprendre-les-cancers-du-sein/developpement-des-cancers-du-sein/les-facteurs-de-risque/predispositions-genetiques
- Le risque familial de cancer du sein et/ou de l’ovaire. Groupe génétique et cancer FNCLCC et La ligue contre le cancer. 2002
- INCa. Les grades du cancer. Mis à jour le 04/11/2020. Consulté le 18/03/2025. Disponible sur : https://www.cancer.fr/personnes-malades/les-cancers/sein/comprendre-les-cancers-du-sein/developpement-des-cancers-du-sein/les-grades-du-cancer